Η καχεξία είναι μια συστηματική νόσος που χαρακτηρίζεται από απώλεια βάρους, ατροφία των μυών και του λιπώδους ιστού και συστηματική φλεγμονή. Η καχεξία είναι μία από τις κύριες επιπλοκές και αιτίες θανάτου σε ασθενείς με καρκίνο. Εκτιμάται ότι η συχνότητα εμφάνισης καχεξίας σε ασθενείς με καρκίνο μπορεί να φτάσει το 25% έως 70% και περίπου 9 εκατομμύρια άνθρωποι παγκοσμίως πάσχουν από καχεξία κάθε χρόνο, το 80% των οποίων αναμένεται να πεθάνει εντός ενός έτους από τη διάγνωση. Επιπλέον, η καχεξία επηρεάζει σημαντικά την ποιότητα ζωής (ΠΖ) των ασθενών και επιδεινώνει την τοξικότητα που σχετίζεται με τη θεραπεία.
Η αποτελεσματική παρέμβαση στην καχεξία έχει μεγάλη σημασία για τη βελτίωση της ποιότητας ζωής και της πρόγνωσης των ασθενών με καρκίνο. Ωστόσο, παρά την κάποια πρόοδο στη μελέτη των παθοφυσιολογικών μηχανισμών της καχεξίας, πολλά φάρμακα που αναπτύχθηκαν με βάση πιθανούς μηχανισμούς είναι μόνο μερικώς αποτελεσματικά ή αναποτελεσματικά. Επί του παρόντος, δεν υπάρχει αποτελεσματική θεραπεία εγκεκριμένη από τον Οργανισμό Τροφίμων και Φαρμάκων των ΗΠΑ (FDA).
Η καχεξία (σύνδρομο απίσχνανσης) είναι πολύ συχνή σε ασθενείς με πολλούς τύπους καρκίνου, με αποτέλεσμα συχνά απώλεια βάρους, μυϊκή ατροφία, μειωμένη ποιότητα ζωής, μειωμένη λειτουργικότητα και βραχύτερη επιβίωση. Σύμφωνα με τα διεθνώς συμφωνημένα πρότυπα, αυτό το πολυπαραγοντικό σύνδρομο ορίζεται ως δείκτης μάζας σώματος (ΔΜΣ, βάρος [kg] διαιρούμενο με ύψος [m] στο τετράγωνο) μικρότερος από 20 ή, σε ασθενείς με σαρκοπενία, απώλεια βάρους μεγαλύτερη από 5% σε έξι μήνες ή απώλεια βάρους μεγαλύτερη από 2%. Επί του παρόντος, δεν έχουν εγκριθεί φάρμακα στις Ηνωμένες Πολιτείες και την Ευρώπη ειδικά για τη θεραπεία της καρκινικής καχεξίας, με αποτέλεσμα περιορισμένες θεραπευτικές επιλογές.
Οι πρόσφατες οδηγίες που συνιστούν χαμηλή δόση ολανζαπίνης για τη βελτίωση της όρεξης και του βάρους σε ασθενείς με προχωρημένο καρκίνο βασίζονται σε μεγάλο βαθμό στα αποτελέσματα μιας μονοκεντρικής μελέτης. Επιπλέον, η βραχυπρόθεσμη χρήση αναλόγων προγεστερόνης ή γλυκοκορτικοειδών μπορεί να προσφέρει περιορισμένα οφέλη, αλλά υπάρχει κίνδυνος ανεπιθύμητων παρενεργειών (όπως η χρήση προγεστερόνης που σχετίζεται με θρομβοεμβολικά επεισόδια). Οι κλινικές δοκιμές άλλων φαρμάκων δεν έχουν δείξει επαρκή αποτελεσματικότητα για να εξασφαλίσουν την έγκριση από τις ρυθμιστικές αρχές. Παρόλο που η αναμορίνη (μια από του στόματος μορφή πεπτιδίων απελευθέρωσης αυξητικής ορμόνης) έχει εγκριθεί στην Ιαπωνία για τη θεραπεία της καρκινικής καχεξίας, το φάρμακο αύξησε μόνο τη σύνθεση του σώματος σε κάποιο βαθμό, δεν βελτίωσε τη δύναμη λαβής και τελικά δεν εγκρίθηκε από τον Οργανισμό Τροφίμων και Φαρμάκων των ΗΠΑ (FDA). Υπάρχει επείγουσα ανάγκη για ασφαλείς, αποτελεσματικές και στοχευμένες θεραπείες για την καρκινική καχεξία.
Ο παράγοντας διαφοροποίησης ανάπτυξης 15 (GDF-15) είναι μια κυτοκίνη που προκαλείται από το στρες και συνδέεται με την πρωτεΐνη άλφα-like (GFRAL) του υποδοχέα της οικογένειας νευροτροφικών παραγόντων που προέρχεται από τη γλοία στο οπίσθιο τμήμα του εγκεφάλου. Η οδός GDF-15-GFRAL έχει αναγνωριστεί ως ένας σημαντικός ρυθμιστής της ανορεξίας και της ρύθμισης του βάρους και παίζει ρόλο στην παθογένεση της καχεξίας. Σε ζωικά μοντέλα, ο GDF-15 μπορεί να προκαλέσει καχεξία και η αναστολή του GDF-15 μπορεί να ανακουφίσει αυτό το σύμπτωμα. Επιπλέον, τα αυξημένα επίπεδα GDF-15 σε ασθενείς με καρκίνο σχετίζονται με μειωμένο σωματικό βάρος και σκελετική μυϊκή μάζα, μειωμένη δύναμη και μειωμένο προσδόκιμο επιβίωσης, υπογραμμίζοντας την αξία του GDF-15 ως πιθανού θεραπευτικού στόχου.
Η ponsegromab (PF-06946860) είναι ένα εξαιρετικά επιλεκτικό ανθρωποποιημένο μονοκλωνικό αντίσωμα ικανό να συνδέεται με την κυκλοφορούσα GDF-15, αναστέλλοντας έτσι την αλληλεπίδρασή της με τον υποδοχέα GFRAL. Σε μια μικρή ανοιχτή δοκιμή φάσης 1b, 10 ασθενείς με καρκινική καχεξία και αυξημένα επίπεδα κυκλοφορούντος GDF-15 έλαβαν ponsegromab και παρουσίασαν βελτιώσεις στο βάρος, την όρεξη και τη σωματική δραστηριότητα, ενώ τα επίπεδα GDF-15 στον ορό αναστέλλονταν και τα ανεπιθύμητα συμβάντα ήταν χαμηλά. Με βάση αυτό, διεξήγαμε μια κλινική δοκιμή Φάσης 2 για να αξιολογήσουμε την ασφάλεια και την αποτελεσματικότητα της ponsegromab σε ασθενείς με καρκινική καχεξία με αυξημένα επίπεδα κυκλοφορούντος GDF-15, σε σύγκριση με το εικονικό φάρμακο, για να ελέγξουμε την υπόθεση ότι η GDF-15 είναι η κύρια παθογένεση της νόσου.
Η μελέτη περιελάμβανε ενήλικες ασθενείς με καχεξία που σχετίζεται με καρκίνο (μη μικροκυτταρικό καρκίνο του πνεύμονα, καρκίνο του παγκρέατος ή καρκίνο του παχέος εντέρου) με επίπεδο GDF-15 ορού τουλάχιστον 1500 pg/ml, βαθμολογία φυσικής κατάστασης Eastern Tumor Consortium (ECOG) ≤3 και προσδόκιμο ζωής τουλάχιστον 4 μηνών.
Οι εγγεγραμμένοι ασθενείς τυχαιοποιήθηκαν για να λάβουν 3 δόσεις ponsegromab 100 mg, 200 mg ή 400 mg ή εικονικό φάρμακο, υποδορίως κάθε 4 εβδομάδες σε αναλογία 1:1:1. Το κύριο καταληκτικό σημείο ήταν η αλλαγή στο σωματικό βάρος σε σχέση με την αρχική τιμή στις 12 εβδομάδες. Το βασικό δευτερεύον καταληκτικό σημείο ήταν η αλλαγή από την αρχική τιμή στην βαθμολογία της Υποκλίμακας Καχεξίας Ανορεξίας (FAACT-ACS), μια αξιολόγηση της θεραπευτικής λειτουργίας για την καχεξία ανορεξίας. Άλλα δευτερεύοντα καταληκτικά σημεία περιελάμβαναν τις βαθμολογίες ημερολογίου συμπτωμάτων καχεξίας που σχετίζονται με τον καρκίνο, τις αλλαγές στην αρχική τιμή στη σωματική δραστηριότητα και τα καταληκτικά σημεία βάδισης που μετρήθηκαν χρησιμοποιώντας φορετές ψηφιακές συσκευές υγείας. Οι ελάχιστες απαιτήσεις χρόνου χρήσης καθορίζονται εκ των προτέρων. Η αξιολόγηση ασφάλειας περιελάμβανε τον αριθμό των ανεπιθύμητων συμβάντων κατά τη διάρκεια της θεραπείας, τα αποτελέσματα εργαστηριακών εξετάσεων, τα ζωτικά σημεία και τα ηλεκτροκαρδιογραφήματα. Τα διερευνητικά καταληκτικά σημεία περιελάμβαναν τις αλλαγές στην αρχική τιμή στον δείκτη των οσφυϊκών σκελετικών μυών (εμβαδόν των σκελετικών μυών διαιρούμενο με το τετράγωνο του ύψους) που σχετίζονται με τον συστηματικό σκελετικό μυ.
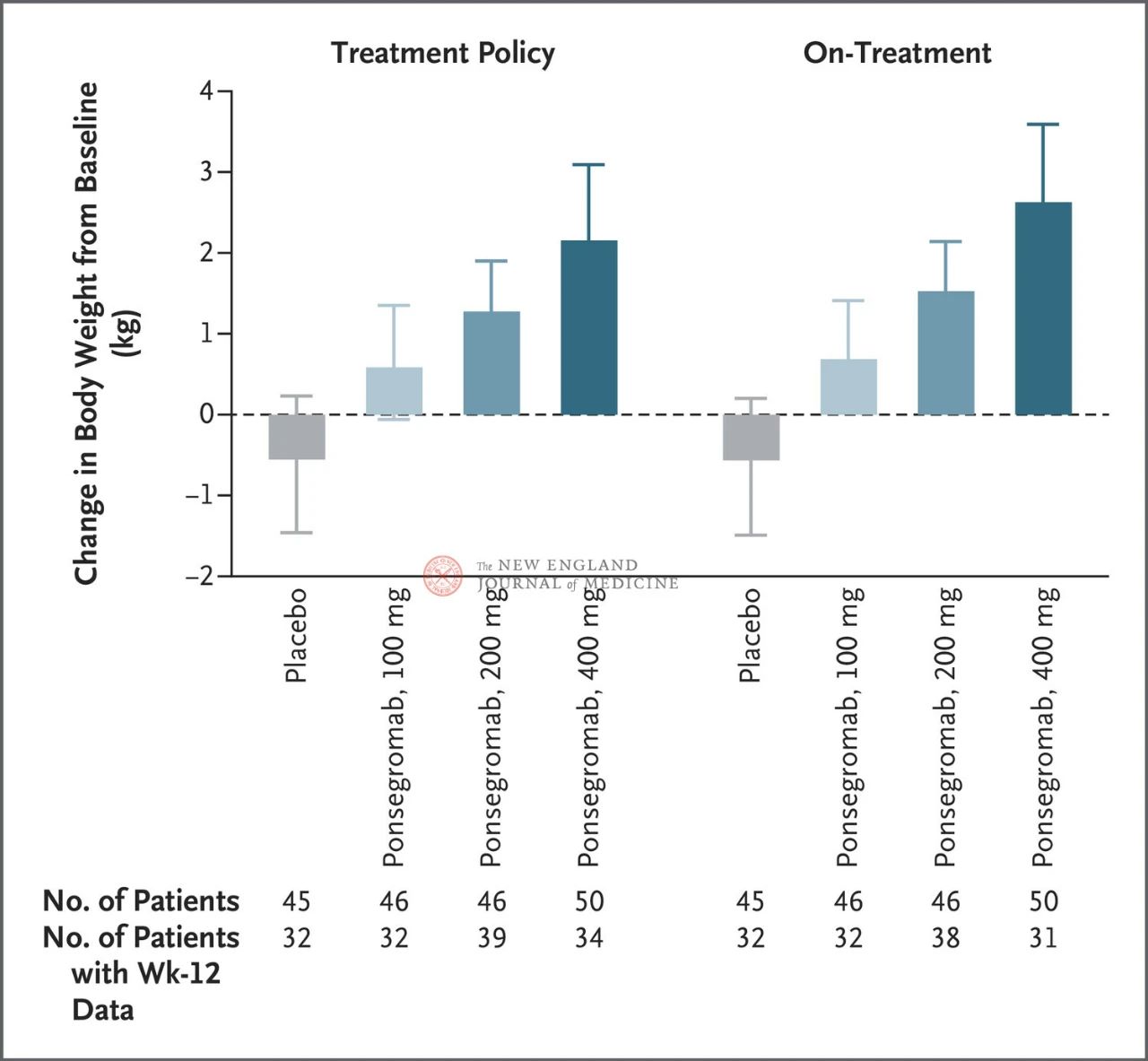
Συνολικά 187 ασθενείς επιλέχθηκαν τυχαία για να λάβουν ponsegromab 100 mg (46 ασθενείς), 200 mg (46 ασθενείς), 400 mg (50 ασθενείς) ή εικονικό φάρμακο (45 ασθενείς). Εβδομήντα τέσσερις (40%) είχαν μη μικροκυτταρικό καρκίνο του πνεύμονα, 59 (32%) είχαν καρκίνο του παγκρέατος και 54 (29%) είχαν καρκίνο του παχέος εντέρου.
Οι διαφορές μεταξύ των ομάδων των 100 mg, 200 mg και 400 mg και του εικονικού φαρμάκου ήταν 1,22 kg, 1,92 kg και 2,81 kg, αντίστοιχα.
Το σχήμα δείχνει το πρωτεύον τελικό σημείο (αλλαγή στο σωματικό βάρος από την αρχική τιμή έως τις 12 εβδομάδες) για ασθενείς με καρκινική καχεξία στις ομάδες ponsegromab και εικονικού φαρμάκου. Μετά την προσαρμογή για τον ανταγωνιστικό κίνδυνο θανάτου και άλλα ταυτόχρονα συμβάντα, όπως η διακοπή της θεραπείας, το πρωτεύον τελικό σημείο αναλύθηκε με ένα στρωματοποιημένο μοντέλο Emax χρησιμοποιώντας αποτελέσματα εβδομάδας 12 από μια Bayesian διαχρονική ανάλυση αρθρώσεων (αριστερά). Τα πρωτεύοντα τελικά σημεία αναλύθηκαν επίσης με παρόμοιο τρόπο, χρησιμοποιώντας εκτιμώμενους στόχους για την πραγματική θεραπεία, όπου οι παρατηρήσεις μετά από όλα τα ταυτόχρονα συμβάντα περικόπηκαν (δεξί σχήμα). Διαστήματα εμπιστοσύνης (υποδεικνύονται στο άρθρο)
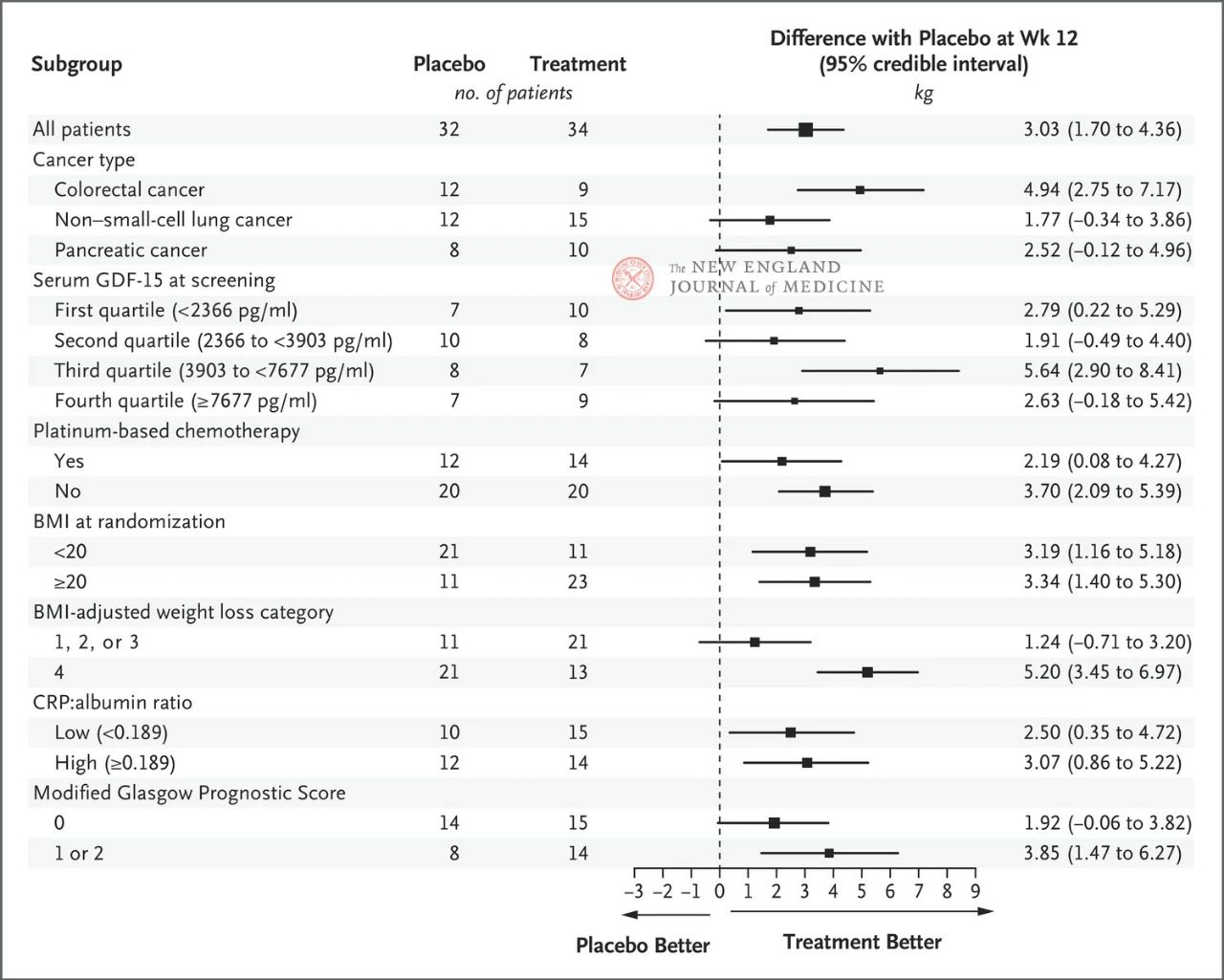
Η επίδραση των 400 mg ponsegromab στο σωματικό βάρος ήταν σταθερή σε όλες τις κύριες προκαθορισμένες υποομάδες, συμπεριλαμβανομένου του τύπου καρκίνου, του τεταρτημορίου των επιπέδων GDF-15 στον ορό, της έκθεσης σε χημειοθεραπεία με βάση την πλατίνα, του ΔΜΣ και της συστηματικής φλεγμονής κατά την έναρξη. Η μεταβολή του βάρους ήταν σύμφωνη με την αναστολή του GDF-15 στις 12 εβδομάδες.
Η επιλογή των βασικών υποομάδων βασίστηκε σε μια post-hoc Bayesian διαχρονική ανάλυση των αρθρώσεων, η οποία διεξήχθη μετά από προσαρμογή για τον ανταγωνιστικό κίνδυνο θανάτου με βάση τον εκτιμώμενο στόχο της θεραπευτικής στρατηγικής. Τα διαστήματα εμπιστοσύνης δεν θα πρέπει να χρησιμοποιούνται ως υποκατάστατο του ελέγχου υποθέσεων χωρίς πολλαπλές προσαρμογές. Ο ΔΜΣ αντιπροσωπεύει τον δείκτη μάζας σώματος, η CRP αντιπροσωπεύει την C-αντιδρώσα πρωτεΐνη και ο GDF-15 αντιπροσωπεύει τον παράγοντα διαφοροποίησης ανάπτυξης 15.
Κατά την έναρξη, ένα υψηλότερο ποσοστό ασθενών στην ομάδα ponsegromab 200 mg δεν ανέφερε μείωση της όρεξης. Σε σύγκριση με το εικονικό φάρμακο, οι ασθενείς στις ομάδες ponsegromab 100 mg και 400 mg ανέφεραν βελτίωση της όρεξης από την έναρξη στις 12 εβδομάδες, με αύξηση στις βαθμολογίες FAACT-ACS κατά 4,12 και 4,5077, αντίστοιχα. Δεν υπήρξε σημαντική διαφορά στις βαθμολογίες FAACT-ACS μεταξύ της ομάδας των 200 mg και της ομάδας εικονικού φαρμάκου.
Λόγω των προκαθορισμένων απαιτήσεων χρόνου χρήσης και προβλημάτων με τη συσκευή, 59 και 68 ασθενείς, αντίστοιχα, παρείχαν δεδομένα σχετικά με τις αλλαγές στη σωματική δραστηριότητα και τα τελικά σημεία βάδισης σε σχέση με την αρχική τιμή. Μεταξύ αυτών των ασθενών, σε σύγκριση με την ομάδα του εικονικού φαρμάκου, οι ασθενείς στην ομάδα των 400 mg παρουσίασαν αύξηση στη συνολική δραστηριότητα στις 12 εβδομάδες, με αύξηση 72 λεπτών μη καθιστικής σωματικής δραστηριότητας ανά ημέρα. Επιπλέον, η ομάδα των 400 mg παρουσίασε επίσης αύξηση στον δείκτη οσφυϊκού σκελετικού μυός την εβδομάδα 12.
Η συχνότητα εμφάνισης ανεπιθύμητων ενεργειών ήταν 70% στην ομάδα της πονσεγκρομάμπης, σε σύγκριση με 80% στην ομάδα του εικονικού φαρμάκου, και εμφανίστηκε στο 90% των ασθενών που έλαβαν ταυτόχρονα συστηματική αντικαρκινική θεραπεία. Η συχνότητα εμφάνισης ναυτίας και εμέτου ήταν χαμηλότερη στην ομάδα της πονσεγκρομάμπης.
Ώρα δημοσίευσης: 05 Οκτωβρίου 2024